Ахалазия пищевода и кардии (кардиоспазм) - симптомы и лечение
Что такое ахалазия пищевода и кардии (кардиоспазм)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Пузанова Сергея Юрьевича, хирурга со стажем в 32 года.
Над статьей доктора Пузанова Сергея Юрьевича работали литературный редактор Елизавета Цыганок, научный редактор Елена Максимова и шеф-редактор Маргарита Тихонова.

Хирург
Cтаж — 32 года
Кандидат наук
Елизаветинская больница на Вавиловых, Поликлиника Елизаветинской больницы
Определение болезни. Причины заболевания
Ахалазия кардии (Esophageal achalasia) — это болезнь, при которой плохо сокращается средний отдел пищевода, а его нижний сфинктер (кардия) не может рефлекторно расслабиться при глотании и открывается механически, под давлением скопившейся пищи [1][2]. По-другому это заболевание называют ахалазией пищевода, спазмом пищевода или кардиоспазмом.
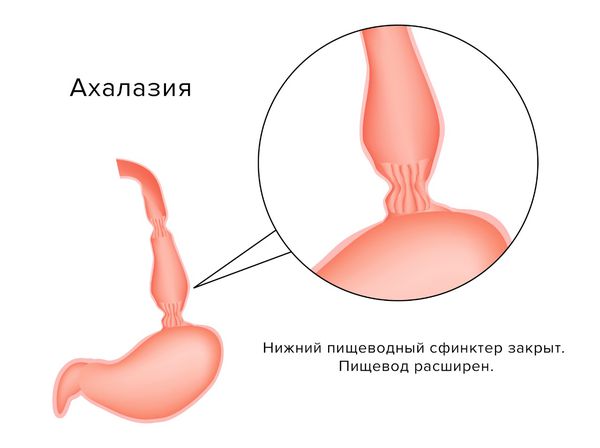
При нормальном состоянии во время глотания кардия (отверстие между пищеводом и желудком) рефлекторно открывается. Однако при ахалазии небольшой участок пищевода лишён нервных клеток, из-за чего пищевод в преддверии желудка стойко и постепенно сужается, а кардия не открывается. В этом случае пища и жидкость скапливаются в пищеводе, после чего клапан не выдерживает давления и еда попадает в желудок.
Распространённость ахалазии пищевода и кардии
Ахалазия кардии встречается редко. Распространённость болезни составляет 10 случаев на 100 тыс. населения, заболеваемость колеблется от 0,1 до 1 случая на 100 тыс. населения [3]. Однако в последние 16 лет в США увеличилось количество госпитализированных пациентов с ахалазией, не достигших 65 лет. Также выросло число людей, у которых ахалазия возникла после того, как они получили травму спинного мозга (обычно травму шейных и грудных отделов позвоночника).
Ахалазия кардии встречается одинаково часто среди мужчин и женщин. Возраст пациентов колеблется от 20 до 50 лет, среди детей, не достигших 16 лет, частота заболеваемости менее 2–5 % [3].
Причины развития ахалазии пищевода и кардии
Считается, что ахалазия возникает в результате поражения мышечно-кишечного сплетения и волокон блуждающего нерва нижнего пищеводного сфинктера. Также в пищеводном межмышечном сплетении нет тормозных нейронов, содержащих вазоактивный интестинальный пептид (ВИП), который улучшает кровоснабжение нервных тканей. В тяжёлых случаях у пациента нет нейронов, передающих нервные импульсы с помощью ацетилхолина.
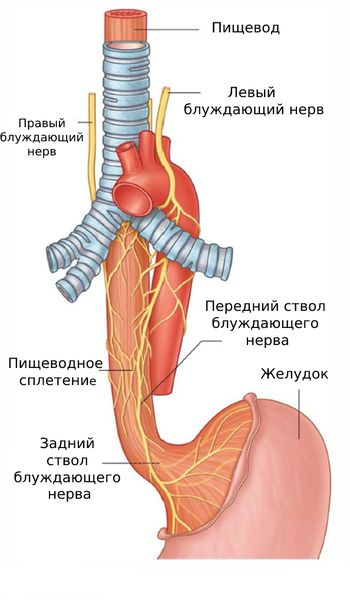
Причины развития болезни до конца не ясны, однако существует несколько теорий, включая аутоиммунный феномен, вирусную инфекцию и генетическую предрасположенность.
Большинство случаев, наблюдаемых в США, представляют собой самостоятельную болезнь, которая возникла без видимой причины. Однако вторичная ахалазия может развиться:
на фоне болезни Шагаса, вызванной одноклеточным паразитом Trypanosoma cruzi;
- проникновения в пищевод клеток карциномы желудка;
- эозинофильного гастроэнтерита;
- лимфомы;
- вирусных инфекций;
- нейродегенеративных болезней (например, болезни Паркинсона, болезни Гентингтона) [13].

При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением — это опасно для вашего здоровья!
Симптомы ахалазии пищевода и кардии
При ахалазии пищевода и кардии выделяют три основных симптома:
- дисфагию — нарушение глотания;
- регургитацию — движение жидкостей и газов в обратную сторону, так называемый заброс;
- боль за грудиной.
К другим немаловажным симптомам ахалазии кардии относят снижение веса, которое встречается примерно у 60% пациентов, и икоту (8%) [1].
Дисфагия
Дисфагия возникает у пациентов с ахалазией в 90–98 % случаев в зависимости от твёрдости пищи [1]. Выделяют две формы дисфагии: острую и прогрессирующую.
Острая дисфагия возникает внезапно и, как правило, у молодых пациентов. Её появление связывают с психотравмирующей ситуацией, например депрессией, тревожным расстройством, последствием инсультов, бредом или шизофренией. В таком случае пациенты могут точно обозначить даты возникновения болезни и связать с событием, которое произошло в этот период. Иногда при острой дисфагии твёрдая пища проходит хорошо, а жидкая задерживается.
На развитие дисфагии также влияет быстрый приём пищи (перекус на ходу), непривычная обстановка во время еды, плохо пережёванная масса и употребление холодных продуктов.
Постепенно прогрессирующая дисфагия обычно встречается у людей среднего и пожилого возраста, т. е. после 40 лет, и развивается в течение долгого времени. Пациент не может точно сказать дату начала болезни, и поэтому у него возникает ощущение, что он болеет всю жизнь [1].
Регургитация
Регургитация встречается в 68–84 % случаев [1]. Различают активную и пассивную регургитацию.
Активная регургитация чаще возникает на ранних стадиях болезни, когда стенки пищевода над сфинктером незначительно расширены. Пища забрасывается обратно в пищевод, после чего пациент срыгивает еду.
При пассивной регургитации пищевод расширяется сильнее. Часто пища забрасывается, когда человек лежит или наклоняется вперёд. В таком случае есть опасность, что еда попадёт в дыхательные пути [1].
Загрудинные боли
Загрудинные боли возникают у 59% пациентов и распространены среди молодых людей до 35 лет [1]. Если боль вызвана высоким давлением в нижнем пищеводном сфинктере, она проявляется приступами. При плохом сокращении мышц пищевода пациенты жалуются на длительные распирающие загрудинные боли. Боль также может вызывать спазм мышц пищевода [1].
Патогенез ахалазии пищевода и кардии
Пищевод не только транспортирует пищевой комок изо рта в желудок, он также предотвращает его обратный заброс. Это происходит благодаря скоординированным сокращениям глотки и пищевода в сочетании с расслаблением верхнего и нижнего пищеводных сфинктеров.
Парасимпатические пути возбуждения и торможения связаны с гладкой мускулатуой нижнего пищеводного сфинктера. Давление и расслабление сфинктера координируют нейромедиаторы. Такие медиаторы делятся на два типа:
- возбуждающие — субстанция Р и ацетилхолин;
- тормозные — ВИП и оксид азота.
У людей с ахалазией отсутствуют тормозные клетки, но возбуждающие нейроны остаются незатронутыми, что приводит к дисбалансу передачи тормозных и возбуждающих нервных импульсов. В результате сфинктер пищевода находится в постоянном напряжении [12].
Постепенная нервная дегенерация напрямую ведёт к чрезмерным сокращениям нижнего пищеводного сфинктера, которые никак не регулируются. В итоге из-за постоянного спазма развивается непроходимость, сам пищевод расширяется и перестаёт сокращаться, а симптомы болезни ухудшаются.
Хотя причина возникновения этих изменений до сих пор остаётся неясной, важное место занимает генетическая предрасположенность. Мутация гена AAAS12q13 у детей ведёт к развитию тройного синдрома ААА, который включают в себя ахалазию, болезнь Аддисона и алакримию, при которой у больного снижается или исчезает выработка слёз. Генетический фактор развития болезни среди взрослых связан с геном IL23R. Такой вывод сделали на основе исследования больных мужчин до 40 лет в Испании [1].
Классификация и стадии развития ахалазии пищевода и кардии
Для описания клинической картины течения болезни часто используют классификацию Б. В. Петровского. В ней выделяют 4 последовательные стадии:
- I стадия — кардия раскрывается и пищевод не расширен, но появляется нарушение координации и усиление его моторики. Возникают первые симптомы: дисфагия и регургитация.
- II стадия — кардия не открывается, пищевод расширен до 4 см. К первым симптомам присоединяется боль в грудной клетке.
- III стадия — пищевод расширяется до 6–8 см, сокращения слабые или отсутствуют, жидкость и пища плохо проходят в желудок. Пациент начинает терять вес.
- IV стадия — размер пищевода становится больше 8 см, из-за долгой задержки пищи и жидкости он удлиняется и приобретает S-образную форму. Стенки пищевода перестают сокращаться [2]. При прогрессировании болезни к симптомам присоединяются проявления застойного эзофагита: тошнота, отрыжка тухлым, повышенное слюноотделение и неприятный запах изо рта [1].
Перечисленные симптомы не всегда напрямую связаны со стадией болезни. Определить её можно только с помощью ЭГДС.
Осложнения ахалазии пищевода и кардии
Среди основных осложнений выделяют:
- Перфорацию пищевода — повреждение стенок пищевода. Сама по себе болезнь встречается редко, но при ахалазии кардии риск развития возрастает. Это связано со скоплением пищи в пищеводе, которая постоянно воздействует на его стенки. Проявлениями этого осложнения являются многократная рвота, боль за грудиной, иногда повышается потоотделение, появляются одышка и симптомы общей интоксикации.
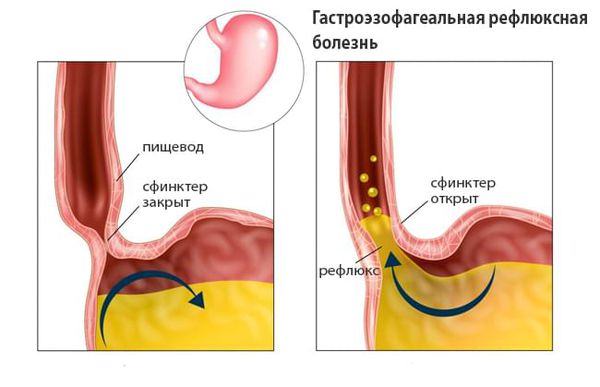
- Гастроэзофагеальную рефлюксную болезн (ГЭРБ) — хроническая болезнь, при которой содержимое желудка и двеннадцатиперстной кишки забрасывается в пищевод. Пациенты жалуются на изжогу, отрыжку с кислым привкусом и боль за грудиной, которая распространяется на область между лопатками, нижнюю челюсть, шею и левую половину груди. Сразу после приёма пищи появляется жжение в груди, оно также возникает, когда пациент наклоняется или ложится.
- Вздутие живота — субъективное ощущение, которое связанно со скоплением газа или чувством давления и растяжения. Для него характерно увеличение и урчание живота, болезненные спазмы и схваткообразные приступы, внезапные отрыжки, тошнота, неконтролируемое выхождение газов с неприятным запахом, тяжесть, частое расстройство стула.
- Застойный эзофагит — воспаление слизистой оболочки пищевода. При застойном эзофагите пациент чувствует дискомфорт, жжение и боль за грудиной, у пациента появляется ощущение комка, застрявшего в горле, могут возникнуть изжога, тошнота, рвота и отрыжка с чувством горечи или кислоты. Долгое течение и отсутствие лечения может привести к формированию раковых клеток [4].
Диагностика ахалазии пищевода и кардии
Перед назначением различных исследований врач уточняет особенности болезни: когда и в связи с чем она появилась, какие возникли симптомы, какие препараты использовались, насколько они были эффективны, есть ли сопутствующие патологии и т. д.
Лабораторная диагностика
Далее врач назначает:
- общий анализ крови — чтобы определить уровень гемоглобина, эритроцитов и лейкоцитов;
- коагулограмму — исследование, которое оценивает состояния системы свёртывания крови, анализы крови необходимы для исключения кровотечения;
- суточный анализ мочи — чтобы определить уровень сывороточного креатинина и альбумина;
- общий анализ мочи — при появлении кетонов врач может сделать вывод о длительности голодания, так как пациент не всегда может дать объективную оценку.
Инструментальная диагностика
При подозрении на ахалазию пищевода и кардии пациент проходит:
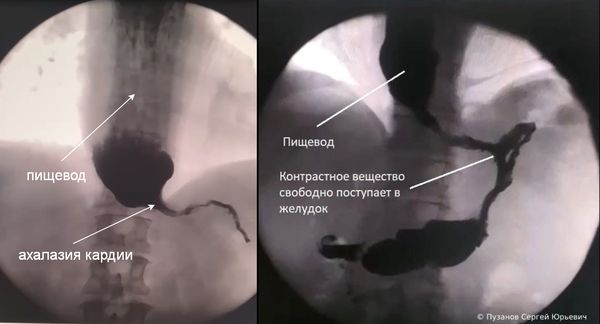
- Рентгенографию с контрастом — в качестве контраста используют бариевую взвесь. В ходе процедуры врач может увидеть расширение и S-образное искривление пищевода, газовый пузырь и момент открытия нижнего пищеводного сфинктера, он также оценивает скорость продвижения контрастной массы [1].
- Эзофагогастродуоденоскопию (ЭГДС) — помогает исключить псевдоахалазии. С помощью этой процедуры можно точно определить степень расширения пищевода и увидеть, есть ли в нём пища.
- Манометрию — позволяет оценить работу пищевода, где главными критериями являются сокращение стенок и давление внутри пищевода. Результаты исследования анализируют с помощью Чикагской классификации нарушений моторики пищевода (2008) [5]. Чтобы получить достоверный результат, перед исследованием нужно сделать 10 глотков воды [14].
Лечение ахалазии пищевода и кардии
Главная цель лечения — облегчить симптомы и уменьшить сопротивление оттоку пищи, которая скапливается в пищеводе из-за постоянно возбуждённого нижнего пищеводного сфинктера.
Консервативное лечение
Чтобы снизить давление в нижнем пищеводном сфинктере, пациенту с ахалазией пищевода и кардии назначают нитраты, блокаторы кальциевых каналов и ингибиторы фосфодиэстеразы-5. Блокаторы кальциевых каналов задерживают поступление кальция в клетки и блокируют сокращение гладкой мускулатуры. Противопоказаниями к применению являются гипотензия, отёк стопы, головная боль, быстрое привыкание к лекарству и неполное улучшение симптомов. Нитраты увеличивают концентрацию оксида азота в гладких мышцах, что приводит к их расслаблению.
Медикаментозное лечение характеризуется слабой эффективностью и обеспечивает лишь кратковременное облегчение симптомов. Как правило, его используют пациенты, которые ожидают или отказались от более радикальной терапии, например пневматического расширения (дилатации) сфинктера или хирургического вмешательства [4][5]. Если пациент отказался от этих способов лечения, лекарства необходимо принимать постоянно. При этом они будут частично устранять симптомы, но полное излечение не наступит.
Эндоскопическую инъекцию ботулинического токсина используют при лечении ахалазии кардии или её рецидива после операции (миотомии). Ботулинический токсин — это мощный биологический нейротоксин, который блокирует высвобождение ацетилхолина на уровне нижнего пищеводного сфинктера. Такое лечение полезно для пациентов, которые не могут сделать операцию или дилатацию, или они используют этот метод в качестве перехода к более радикальной терапии. Однако эффективность инъекции со временем снижается:
- в течение месяца эффективность составляет 80%;
- через 3 месяца — 70%;
- через 6 месяцев — около 50%;
- через год — 40%.
Это приводит к тому, что иногда пациенту требуется повторная инъекция ботулотоксина.
Пневматическая дилатация пищевода с помощью эндоскопии — это наиболее экономически выгодный нехирургический метод лечения ахалазии. При пневматической дилатации давление воздуха постепенно расширяет пищевод и разрывает циркулярные волокна сфинктера. Этот метод помогает 50–93% пациентов, но у 30% симптомы появляются снова через 5 лет [7]. В некоторых случаях повторная дилатация обеспечивает длительную ремиссию.
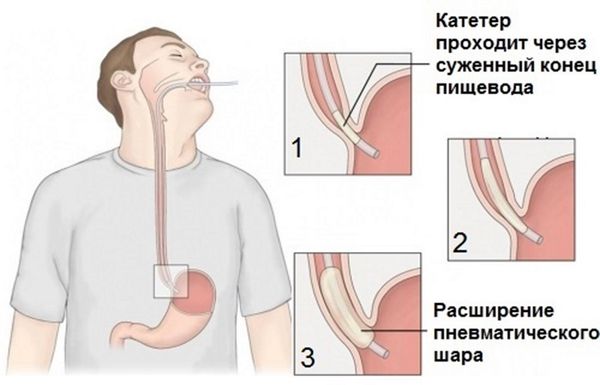
Наиболее распространённые осложнения, связанные с процедурой, незначительны, но иногда возникают серьёзные осложнения, которые также следует лечить, например перфорация пищевода.
Пневматическая дилатация — первый вариант лечения после неэффективной операции. Если пневматическая дилатация также не приносит результата, перед повторной манипуляцией врач ищет причину с помощью инструментальных методов диагностики (рентген и ЭГДС) [9].
Противопоказаниями для дилатации являются:
- общее тяжёлое состояние пациента (острый инфаркт, инсульт);
- пищеводно-респираторные свищи, так как манипуляция может привести к увеличению свищевого хода;
- полное заращение или сужение просвета органа/анастомоза из-за сдавливания извне (например, злокачественной опухолью или рубцовым процессом на фоне лучевой терапии), при котором гибкий проводник не может пройти через суженый просвет пищевода;
- портальная гипертензия и варикозное расширение вен пищевода.
Хирургическое лечение
Чтобы снизить давление на нижний сфинктер, врачи рекомендуют пройти лапароскопическую миотомию. В ходе процедуры хирург рассекает круговые мышечные волокна, которые проходят через сфинктер, в результате чего он расслабляется [10].
Лапароскопическая миотомия по Геллеру (ЛМГ) является одним из вариантов оперативного лечения ахалазии. Её проводят с фундопликацией — антирефлюксной процедурой, при которой дно желудка оборачивают вокруг пищевода. Такую фундопликацию делают только частично, чтобы не вызвать послеоперационную дисфагию.
Уровень клинического успеха ЛМГ высок — от 76 до 100% через 35 месяцев, при этом уровень смертности составляет 0,1% [11]. Специфических противопоказаний у операции нет, кроме общих противопоказаний к любой операции. После процедуры пациенты восстанавливаются около 3 суток.
Пероральная эндоскопическая миотомия (ПОЭМ) — альтернатива ЛМГ с минимальным вмешательством внутрь организма. Её используют для лечения ахалазии в ограниченных очагах. С помощью эндоскопа врач рассекает циркулярные волокна нижнего сфинктера и расслабляет его. Однако в этом случае повышается риск развития гастроэзофагеального рефлюкса, поскольку операция не включает в себя антирефлюксную процедуру. Восстановление после операции длится около 2 дней.
Эзофагэктомию — операцию по удалению части пищевода — проводят в крайнем случае [1][8].
Прогноз. Профилактика
Сегодня нет такого метода лечения ахалазии кардии, который давал бы 100%-й результат выздоровления [1]. Поэтому важно соблюдать все рекомендации врача, направленные на предупреждение рецидива: следить за весом, отказаться от острой, кислой, сильно солёной, жареной и копчёной пищи, исключить газированные напитки, не есть твёрдую еду перед сном. Принимать пищу нужно в вертикальном положении или под углом в 45°.
Несмотря на эффективность лечения и устранение симптомов, всегда остаётся высокая вероятность рецидива, поэтому пациенту необходимо раз в год проходить осмотр у гастроэнтеролога [12].
Профилактика ахалазии пищевода и кардии
Чтобы минимизировать риск развития ахалазии, следует:
- нормализовать режим питания — принимать пищу 5–6 раз в день, но небольшими порциями;
- соблюдать специальную диету – отказаться от фастфуда, острой, солёной, жирной и жареной пищи;
- тщательно пережёвывать еду, прежде чем глотать;
- отказаться от вредных привычек (употребления алкоголя и курения);
- заниматься физкультурой;
- больше гулять на свежем воздухе;
- соблюдать режим труда и отдыха;
- избегать физического и эмоционального перенапряжения.
Список литературы
- Ивашкин В. Т., Трухманов А. С., Годжелло Э. А. и др. Рекомендации Российской гастроэнтерологической ассоциации по диагностике и лечению ахалазии кардии и кардиоспазма // РЖГГК. — 2016. — № 4. — С. 36–54.
- Гаджиев А. Н. Клиника, диагностика, лечение кардиоспазма, ахалазии кардии и диффузного эзофагоспазма: дис. … д-ра мед. наук: 14.00.27. — М., 2001.
- Wadhwa V., Thota P. N., Parikh M. P., Lopez R., Sanaka M. R. Changing Trends in Age, Gender, Racial Distribution and Inpatient Burden of Achalasia // Gastroenterology Res. — 2017. — № 2. — Р. 70–77. ссылка
- Eckardt A. J., Eckardt V. F. Current clinical approach to achalasia // World J Gastroenterol. — 2009. — № 32. — Р. 3969–3975.ссылка
- Torresan F., Ioannou A., Azzaroli F., Bazzoli F. Treatment of achalasia in the era of high-resolution manometry // Ann Gastroenterol. — 2015. — № 3. — Р. 301–308.ссылка
- Zaninotto G., Annese V., Costantini M. et al. Randomized controlled trial of botulinum toxin versus laparoscopic heller myotomy for esophageal achalasia // Ann Surg. — 2004. — № 3. — Р. 364–370.ссылка
- Csendes A., Braghetto I., Henríquez A., Cortés C. Late results of a prospective randomised study comparing forceful dilatation and oesophagomyotomy in patients with achalasia // Gut. — 1989. — № 3. — Р. 299–304. ссылка
- Boeckxstaens G. E., Annese V. et al. European Achalasia Trial Investigators. Pneumatic dilation versus laparoscopic Heller’s myotomy for idiopathic achalasia // N Engl J Med. — 2011. — № 19. — Р. 1807–1816. ссылка
- Галлингер Ю. И., Годжелло Э. А. Оперативная эндоскопия пищевода. — М.: РНЦХ РАМН, 1999. — 273 с.
- Петровский Б. В. Кардиоспазм и его хирургическое значение: труды 27-го Всесоюзного съезда хирургов. — М., 1962. — С.162–173.
- Черноусов А. Ф., Чернявский А. А. Показания к хирургическому лечению кардиоспазма // Хирургия. — 1986. — № 5. — С. 28–32.
- Raymond L., Lach B., Shamji F. M. Inflammatory aetiology of primary oesophageal achalasia: an immunohistochemical and ultrastructural study of Auerbach’s plexus // Histopathology. — 1999. — № 5. — Р. 445–453. ссылка
- Francis D. L., Katzka D. A. Achalasia: update on the disease and its treatment // Gastroenterology. — 2010. — № 2. — Р. 369–374. ссылка
- Кайбышева В. О., Никонов Е. Л., Бордин Д. С., Морозов С. В. и др. Манометрия пищевода высокого разрешения: методические рекомендации. — М., 2018. — 53 с.
